Нейтрофильное воспаление у кошек: описание заболевания, причины, симптомы
Обновлено: 12.05.2024
Общий анализ крови, бесспорно, - самый популярный из всех существующих анализов. И не спроста, ведь его возможности, среди прочего, позволяют выявлять не только наличие и степень воспаления, но и определить его «происхождение» по отношению к возбудителю. А значит и выбор в пользу антибактериальной или противовирусной терапии можно сделать в самые первые дни воспаления, что не только ускорит выздоровление, но и позволит значимо снизить риск серьезных осложнений.
Что такое нейтрофилы и их функции в организме
Нейтрофилы - это гранулоцитарные лейкоциты. Белые клетки крови такого вида наиболее многочисленны. Главная функция нейтрофилов в организме - защита животного от инфекций, вызванных бактериями и грибками.

ИНТЕРЕСНО! Белые клетки крови этого вида более эффективно защищают организм кошки от грибков и бактерий, чем от вирусов.
Если в ткани проникли патогенные микроорганизмы, белые клетки крови устремляются к очагу, разрушают и поглощают грибки и бактерии. Нейтрофилы способны покидать кровяное русло для того, чтобы уничтожить проникшие в организм чужеродные частицы, но при этом они погибают сами.
Лейкоцитарные отряды
Для людей «непосвященных», общий анализ крови с лейкоцитарной формулой (1.0.D2.202) чаще всего похож на «китайский язык». Найти «предложение» о природе воспаления, в котором, на первый взгляд, кажется совершенно невозможным. Тогда как на самом деле, для первичного выяснения характера инфекции, чаще достаточно и «беглой» оценки численности различных представителей лейкоцитов.
1. Нейтрофилы
«Группой моментального реагирования» в борьбе с бактериями являются нейтрофилы, относительное (в %, по отношению к другим разновидностям лейкоцитов) повышение которых в общем анализе крови является надежным маркером любого бактериального воспаления и, соответственно, обоснованием в пользу антибактериального характера лечения.
Тогда как абсолютное увеличение численности нейтрофилов (клеток на литр крови) – чаще сопровождает достаточно тяжелые формы инфекций.
Эти представители лейкоцитов самыми первыми мигрируют из крови в очаг воспаления, где буквально «поедают» и «переваривают» врага с помощью «ядовитых» гранул.
Правда после такого «перекуса», нейтрофилы и сами оказываются нежизнеспособны и погибают. А клиническим отражением этого процесса является образование гноя в очаге воспаления.
2. Лимфоциты
Одновременно с увеличением нейтрофилов, в крови «бактериального» больного наблюдается относительное (в %) снижение основных борцов с вирусами – лимфоцитов, что является отражением нормального перераспределения «иммунных активов» под текущие задачи защиты. А сам процесс имеет название «относительной лимфопении».
3. Моноциты
В качестве «ликвидаторов последствий» воспаления, в очаг из крови «стягиваются» моноциты. Которые уже «на месте» трансформируются в более крупные – макрофаги, и эффективно очищают «пространство» от разрушенных клеток и бактерий.
Максимальное повышение моноцитов в общем анализе крови обычно наблюдается только в самом конце воспаления, как маркер завершения процесса и начала периода восстановления.
А, помимо прочего, моноциты - «солдаты» универсального назначения, и задействованы как при бактериальном, так и вирусном (особенно герпетического происхождения), а также аутоиммунном и некоторых других механизмах воспаления. Поэтому их повышение в той или иной степени характерно практически для всех видов воспалительного процесса.
Нейтрофильное воспаление у кошек сопровождает любую бактериальную или грибковую инфекцию. Белые клетки крови уничтожают чужеродные частицы, однако при этом происходит массовая гибель нейтрофилов в очаге поражения.
Особенности нейтрофильной фазы воспалительных процессов
У нейтрофильной фазы воспалительных процессов существуют свои особенности. При попадании в организм бактерий или грибков запускается процесс программируемой клеточной гибели, при этом нейтрофилы выбрасывают особую внеклеточную ловушку. Это явление называется «нетоз».
После того, как в организм проникли патогенные микроорганизмы, нейтрофилы устремляются к очагу поражения.
После этого происходит следующее:
- Из внутриклеточного органоида (эндоплазматического ретикулума) происходит выход кальция.
- Разрушаются внутренние мембраны нейтрофила.
- Происходит массовая деконденсация (раскручивание молекулы) хроматина (основа хромосом, состоящая из белка, РНК и ДНК).
- Резко повышается уровень АФК (активных форм кислорода).
- Смешиваются антибактериальные белки, нуклеоплазма и цитоплазма, содержащиеся в нейтрофиле, благодаря чему формируется будущая ловушка внутри клетки.
- Плазматическая мембрана разрывается, и получившаяся ловушка выбрасывается за пределы нейтрофила.
Ловушка, которая образуется в результате нетоза, имеет вид трехмерной сети. Ее основа - нити ДНК, на которых находятся антимикробные белки. Такие нити могут сплетаться в более толстые «кабели», и в результате образуется большой клубок. Патогенные микроорганизмы (бактерии и грибки) застревают в этой сети и погибают под воздействием белков.

Такие ловушки быстро и эффективно задерживают бактерии, проникшие в организм кошки, а затем уничтожают их. Однако у этого процесса есть особенность - при аутоиммунных заболеваниях, астме и некоторых воспалительных болезнях выброшенные нейтрофилами сети травмируют соседние клетки, и воспаление прогрессирует, но патогенные микроорганизмы при этом погибают.
Ученые сравнивают механизм действия нейтрофилов с пауками. Иммунные клетки, подобно паукам, закрепляют сеть и устремляются в сторону от нее. За нейтрофилом продолжает тянуться и распускаться ДНК. На эти сети натыкаются другие иммунные клетки и тоже начинают «плести сеть».
В результате даже маленькое количество нейтрофилов способны совместно сплести довольно большую ловушку, в которую попадают чужеродные частицы.
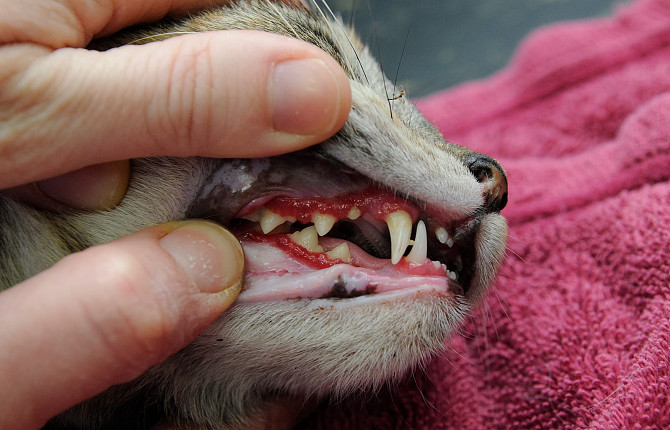
Кошачий гингивостоматит, вероятно, является самым неприятным заболеванием полости рта, наблюдаемым в ветеринарной практике. Оно является чрезвычайно болезненным состоянием для кошки и болезненным состоянием для владельца животного. Слизистая оболочка полости рта, особенно на задней поверхности (иногда называемая зев, но более правильно называть язычно - небные складки) - становится воспаленной и красной и может даже кровоточить.
Заболевшие кошки проявляют различные клинические признаки: анорексии, из-за отказа есть корм (избегая жестких частей пищи), птиализм, галитоз, потеря веса, аномальное глотание и боль в полости рта. При клиническом осмотре, можно обнаружить: гингивит, стоматит, воспаление слизистой оболочки неба, глоссит, хейлит, фарингит, иногда мандибулярную (нижнечелюстную) лимфаденопатию. Участки воспалительного процесса часто обширные, а пораженные ткани, как правило, изъязвленные, пролиферативные и гиперемированы. Когда гингивостоматит был впервые описан, породистые кошки были первые в группе риска, но со временем стало понятно, что все породы кошек имеют потенциал для развития данного заболевания, в том числе домашние беспородные кошки (метисы). Животные подвержены этому заболеванию в любом возрасте.
Хорошая новость заключается в том, что большинство пациентов с гингивостоматитом могут быть вылечены или, по крайней мере, показать заметное улучшение состояния на фоне лечения. Но, к сожалению, некоторым пациентам потребуется пожизненная терапия.
Поражения полости рта, связанные гингивостоматитом у кошек, часто принимают за оральную инфекцию; однако гингивостоматит - это не инфекция, а воспаление. Считается, что воспалительные поражения, связанные с гингивостоматитом кошек, являются результатом высокореактивной иммунной системы. Специфический антиген, на который иммунная система реагирует, не так легко определить и часто он неизвестен. В большинстве случаев удаление всех зубов у кошки приносит положительный эффект, т.е. когда зубы удаляются предполагается удаление антигена, который связан с зубным налетом (бактерионоситель.) Однако, поскольку не все воспаления купируются с помощью удаления зубов, необходимо признать, что могут быть задействованы несколько антигенов. Другие антигены, которые могут иметь роль и вызывать воспаление, связанное с гингивостоматитом включают в себя вирусную природу, пищу, или экологические антигены. Аутоиммунные заболевания также могут быть частью данной болезни.
Дифференциальные диагнозы при воспалениях в ротовой полости у кошек включают - кошачий гингивостоматит, пародонтоз, вторичное воспаление при одонтокластических резорбтивных поражениях зубов кошек (FORLs), некоторые вирусные заболевания (герпесом и/или калицивирусом), которые могут вызвать воспаление в полости рта и язвы на слизистой оболочке, эозинофильную гранулему и неоплазию. Полное диагностическое обследование пациента имеет первостепенное значение для постановки правильного диагноза и начала определенного пути лечения.
Чтобы начать эту оценку, необходимо выполнить физикальное обследование, общий и биохимический анализы крови, а также серологическое тестирование на вирус лейкоза кошек и вирусного иммунодефицита кошек.
Постановка диагноза так же потребует проведение ряда исследований под седацией (анестезией). Необходимо выполнить рентгенографическое исследование полости рта. Экстирпировать зубы которые подвержены резорбции и зубы с заболеваниями периодонта. Также, извлекаются все части корня/корней (если таковы будут определенны рентгенографически). И, наконец, получить образцы воспаленной ткани с помощью биопсии в нескольких местах и представить их для гистологического исследования.
Результаты гистологического исследования у кошек с кошачьим гингивостоматитом показывают плазмоцитарный стоматит или лимфоцитарно - плазмоцитарный стоматит. Может наблюдаться одновременное нейтрофильное воспаление или даже поверхностный бактериальный компонент, но преобладающей популяцией клеток будут плазмоциты и лимфоциты.
В редких случаях, просто поддержание гигиены полости рта будет удерживать это состояние под контролем. Программа ухода на дому может включать ежедневную чистку зубов и применение раствора Мирамистина (местно), а также долгосрочную или долгосрочно - прерывистую (пульсовую) антибиотикотерапию. Антибиотики, спектр действия которых включает грамотрицательные анаэробные бактерии, являются хорошим выбором. Антибиотикотерапия часто дает благоприятные результаты на начальном этапе; однако преимущества антибиотикотерапии, по-видимому, уменьшаются с течением времени. Кошки, у которых данное заболевание наблюдается в течение длительного времени, как правило, являются самыми неперспективными пациентами для домашнего ухода. Если уход на дому сам по себе не работает или невозможен, необходимо рассмотреть возможность медицинского или хирургического лечения.
К сожалению, медикаментозные методы лечения включают лекарства с низкими шансами на успех или препараты с серьезными побочными действиями (например, кортикостероиды.) Было опробовано большое количество препаратов для местных обработок пораженных тканей в ротовой полости с разной степенью эффективности. Долгосрочное использование кортикостероидов не идеально потому что у кошек могут появиться серьезные побочные эффекты, включая сахарный диабет и ятрогенный гиперадренокортицизм. Избегание кортикостероидов особенно важно при лечении животных, инфицированных вирусом иммунодефицита кошек.
Хирургическое лечение
Экстракция всех зубов (или иногда только моляров и премоляров) может принести положительный результат в лечении каудального гингивостоматита кошек. В одном из исследований 60% пациентов с данной патологией, которым провели экстракцию, были излечены клинически, а еще у 20% было значительное улучшение состояния. Эта процедура является трудоемкой и не будет успешной, если остались какие-либо фрагменты корней зубов. Перед выполнением экстракции настоятельно рекомендовано иметь все необходимое оборудование. Наличие стоматологического рентгенографического оборудования и специализированных приборов нельзя переоценить. Невозможно обойтись и без предоперационного и послеоперационного мониторинга и поддержки пациентов, а также соответствующую анальгезию. Пациентов с гингивостоматитом, требующих хирургического лечения, как правило, направляют к ветеринарному специалисту.
При удалении зубов для лечения гингивостоматита возникает вопрос, следует ли экстирпировать резцы и клыки. Рекомендуется удаление резцов и клыков, если они больны или если окружающие ткани заметно воспалены. Если резцы и клыки здоровы и воспаление ограничено каудальной частью полости рта эти зубы можно сохранить.
Затяжной гингивостоматит
Даже после того, как все зубы и корни удалены, около 20% пациентов будут продолжать испытывать боль и будут сохраняться признаки воспаления ротовой полости. В этих случаях является затяжным, и пациенты могут нуждаться в лечении на протяжении всей жизни. В затяжных случаях, никакая из предложенных терапий не работает последовательно, но можно использовать несколько обработок для улучшения качества жизни м уменьшения дискомфорта.
Необходимо повторное рентгенографическое исследование зубных дуг, чтобы исключить сохраненные фрагменты корня или реактивную ткань пародонта. Если клыки или резцы пациента не были изначально удалены, их необходимо удалить сейчас.

Панкреатит кошек часто сопровождается сопутствующими заболеваниями других органов и систем. Патологические нарушения включают липидоз печени, воспалительные болезни печени, обструкцию желчевыводящего тракта, сахарный диабет, воспалительные заболевания ЖКТ, гиповитаминоз (В12, фолата, витамина К), кишечную лимфому, нефриты, лёгочную тромбоэмболию и плевральный или перитонеальный выпот. Термин триадит применяется при комплексе воспалительных заболеваний поджелудочной железы, печени и тонкого отдела кишечника. Триадит обнаруживается в 50-56% у кошек с диагнозом панкреатит и в 32-50% у кошек с диагнозом холангит\воспалительное заболевание печени. Дифференциальная диагностика триадитов основана на гистопатологических исследованиях этих органов. Однако индивидуальное состояние каждого органа определяет диагноз триадит среди других дифференциальных диагнозов. В то время как этиопатогенез панкреатита и его отношение к воспалению других систем органов неоднозначно, первый этап дифференциальной диагностики включает исследование причин воспаления, иммунного ответа и кишечной микрофлоры.
Введение
Панкреатит кошек часто сопровождается сопутствующими заболеваниями других органов и систем. Патологические нарушения включают липидоз печени, воспалительные болезни печени, обструкцию желчевыводящего тракта, сахарный диабет, воспалительные заболевания ЖКТ, гиповитаминоз (В12, фолата, витамина К), кишечную лимфому, нефриты, лёгочную тромбоэмболию и плевральный или перитонеальный выпот. Термин триадит применяется при комплексе воспалительных заболеваний поджелудочной железы, печени и тонкого отдела кишечника. Триадит обнаруживается в 50-56% у кошек с диагнозом панкреатит и в 32-50% у кошек с диагнозом холангит/воспалительное заболевание печени. Эта статья предоставляет обзор причин и лечения панкреатитов и триадитов у кошек, и глубокого рассмотрения этиопатогенеза триадитов.
Дифференциальная диагностика триадитов основана на гистопатологическом исследовании отдельного органа. Однако диагноз триадит включает в себя комбинацию воспалительных изменений, таких как хронический панкреатит, хронический холангит/холангиогепатит и ВЗК. Необходимо соблюдать осторожность при постановке диагноза, делая выводы о причинах триадита, так как прижизненная диагностика затруднительна, а окончательный диагноз ставится посмертно. Диагностика затрудняется различием гистологической классификации и оценки панкреатита кошек, воспалительных заболеваний печени и кишечника, которые могут осложняться стадийностью и корреляцией специфических подтипов болезней этих органов, с триадитами. Стандартизация критериев гистопатологических исследований печени и кишечника может быть затруднена.
Таблица №1. Симптомы, указывающие на триадит
Диагности-
ческие тесты
Панкреатиты
Болезни печени
Воспали-
тельные заболевания кишечника
Диагностика панкреатитов и триадитов
Диагноз триадит, симптомы которого описаны в таблице 1, ставится при наличии комплекса воспалительных заболеваний кишечника, печени и поджелудочной железы. Клинические находки различны и включают: анорексию, потерю веса, потерю мышечной массы, диарею, рвоту, желтуху, гепатомегалию, утолщение стенок кишечника, увеличение поджелудочной железы, абдоминальную боль, абдоминальный выпот, лихорадку, гипотермию, тахипноэ, и шок. Гематологические и биохимические изменения, связанные с болезнями печени — увеличение концентрации АЛТ, АСТ, ГГТ, ЩФ и билирубина; с болезнями поджелудочной железы — увеличение панкреатической липазы и иммунореактивной панкреатической липазы, снижение уровня кальция; с ВЗК или алиментарной лимфомой — недостаток кобаламина, фолата и альбумина. При ультразвуковом исследовании поджелудочной железы отмечают: изменение размера, эхогенности тканей и протока поджелудочной железы; печени: изменение размера и контура органа, эхогенности тканей, состояния желчевыводящей системы; тонкого кишечника: утолщение стенки кишечника и гипертрофия мышечного слоя. Окончательная постановка диагноза требует проведения биопсии и гистопатологического исследования тканей каждого органа.
Схема №1

Каковы причины панкреатита?
Этиопатогенез панкреатита и его осложнений описан в схеме 1. Причины, которые являются пусковым механизмом для развития панкреатита кошек (таблица 2), обычно не очевидны. При этом острый панкреатит может перетекать в хронический, который в свою очередь может сопровождаться экзокринной недостаточностью поджелудочной железы; вероятно, каждая из причин может провоцировать развитие самостоятельного заболевания. Острый панкреатит сопровождается отёком и некрозом, с гипоперфузией и тромбозом, который в свою очередь может усиливать панкреонекроз. Часто панкреатитам сопутствует воспаление тонкого отдела кишечника. Особенно плохой прогноз у гнойного панкреатита. Абсцессы (стерильные и инфицированные) и псевдокисты (возникают из-за локального скопления секрета поджелудочной железы) встречаются редко. Сочетание этих факторов может сопровождаться бактериальной инфекцией и билиарной обструкцией. Бактериальная инфекция может проникать в поджелудочную железу через её проток по восходящему пути или гематогенным путём из кишечника. FISH-исследование (fluorescence in situ hybridisation) обнаруживает бактерий в поджелудочной железе у 13/46 кошек с панкреатитами. Бактериальная инфекция провоцирует более тяжёлые панкреатиты по отношению к случаям, протекающим без неё. Бактериальные колонии чаще обнаруживают в тканях окружающих проток поджелудочной железы, паренхиме органа, окружающем сальнике, участках некроза и выводящих протоках. Хронический панкреатит может приводить к обструкции протока поджелудочной железы и билиарной системы, что в свою очередь ухудшает элиминацию бактерий в печени.
Таблица 2. Возможные причины панкреатита, воспалительных заболеваний печени и ВЗК
Причина
Панкреатит
Воспалительные заболевания печени
Воспалительные заболевания кишечника
Как панкреатит связан с триадитом?
Воспаление в кишечнике, печени и поджелудочной железе может быть обусловлено отдельным патологическим процессом на каждом участке или иметь общую причину. Наиболее вероятные причины воспаления ПЖ, печени и кишечника указаны в схеме 2. Бактериальная инфекция, иммуно-опосредованный ответ и идиопатический механизмы могут также являться потенциальной причиной воспаления каждого органа или провоцировать триадит. При рассмотрении причин триадитов возможно несколько моделей развития заболевания.
Острый панкреатит как причина триадита?
Острое воспаление поджелудочной железы является одним из пусковых механизмов триадита, а также влияет на состояние печени и кишечника (схема 2 А). В этом сценарии панкреатит провоцирует воспаление кишечника через контакт с двенадцатиперстной и толстой кишкой и/или связанных с ними синдромом системного воспалительного ответа, что также способствует дисбиозу и миграции бактерий в поджелудочную железу, минуя воспалённую стенку кишечника или через панкрео-билиарный проток. Комбинация панкреатита и миграция кишечных бактерий приводит к развитию гепатопатии, нейтрофильному холангиту или гепатиту и септицемии. Культуральные исследования чаще выявляют кишечные бактерии в тканях печени и желчи у котов с холангитами и холангиогепатитами. FISH-исследование выявляет бактерий (преобладают E.coli и Streptococcus spp.) в тканях фиксированных формалином, у кошек с воспалительными заболеваниями печени и панкреатитами. У 6-7% «FISH-положительных» кошек с заболеванием печени и у 79% «FISH-положительных» кошек с панкреатитом выявлены воспаления поджелудочной железы, печени и тонкого кишечника. Кроме того, у животных с экспериментальным панкреатитом демонстрировалось, что E. Coli может перемещаться в тонкий отдел кишечника. Появление гипогликемии и ухудшение прогноза может быть связано с развитием гнойного панкреатита, вследствие развития инфекции и сепсиса.
Схема №2

Воспаление кишечника и аутоиммунные причины триадита
Альтернативный этиологический фактор триадита может находиться в кишечнике. В основе этого сценария лежит лимоцитарно-плазмацитарное воспаление или мелкоклеточная лимфома, которые могут сопровождаться дисбиозом и миграцией кишечных бактерий в поджелудочную железу, минуя воспалённую стенку кишечника или панкреобилиарный сосочек.
Повышение интрадуаденального давления ведёт не только ко рвоте, но и к рефлюксу содержимого кишечника в панкреобилиарный проток, приводящий к бактериальному инфицированию печени и поджелудочной железы (схема 2 В). Мы можем обнаружить бактерии в желчи и панкереобилиарном тракте. Однако, бактерии при инфекционных заболевания печени чаще локализуются в портальной вене, венозных синусах и паренхиме (12/13), чем в желчевыводящем тракте(1/13) и только у 3 из 13 кошек с панкреатитом инфекция локализуется в протоке поджелудочной железы. Предполагают, что гематогенный путь развития инфекции более вероятен, чем инфицирование тканей по восходящему пути панкреобилиарных протоков.
Модели, описанные в схеме 2 А, В, наиболее применимы к кошкам с триадитами, панкреатитами средней и тяжёлой степени, воспалительными заболеваниями печени (которые подразделяются на реактивную гепатопатию, нейтрофильный или обструктивный холангиты). Эти кошки чаще имеют активную колонизацию бактерий, чем кошки с более лёгкой формой течения заболеваний.
У кошек с хроническим лимфоцитарным панкреатитом или холангитом редко обнаруживают бактериальную инфекцию, а также наличие ДНК видов Helicobacter, которые вызывают заболевания у других видов животных (у кошек это не доказано). Следовательно, комбинация лимфоцитарного (хронического) панкреатита, лимфоцитарного или смешанного лимфоцитарного и нейтрофильного холангита, и лимфоцитарно-плазмоцитарного энтерита чаще вызвана иммуно-опосредованным ответом, чем бактериальной инфекцией (схема 2 С). В организме человека и экспериментальных животных аутоиммунный панкреатит и холангит возникает как осложнение ВЗК с иммунной атакой на панкреобилиарный тракт. Несколько экспериментальных исследований подтверждают возможность того, что иммунный ответ на кишечных бактерий связан с иммуно-опосредованным панкреатитом и холангитом. Например, C57BL/6 мыши, которым внутрибрюшинно вводят термоинактивированную E. Coli еженедельно в течение 8 недель, показывают выраженную клеточную инфильтрацию и фиброз поджелудочной железы, сопровождающийся повышением концентрации гамма-глобулина в сыворотке крови и образованием аутоантител против карбоангидразы и лактоферрина. Более поздние исследования выявили жгутиковые одноклеточные организмы, FliC из E. Coli, которые являются антигенным стимулом и вызывают повышение титра антител в сыворотке крови у больных иммуно-опосредованным панкреатитом. Экспрессия антигенов хозяина может формировать иммунный ответ. Муцин 1 (MUC1) сверхэкспрессируется в патогенную, гипергликозилированную форму на эпителии толстого отдела кишечника человека с ВЗК, где он провоцирует воспаление. MUC1 так же воздействует на эпителий протока поджелудочной железы. У мышей с ВЗК были выявлены MUC1-специфические Т-клетки, мигрирующие в толстый отдел кишечника и поджелудочную железу. Это говорит о том, что вначале внекишечная часть ВКЗ характеризуется провоспалительной патогенной экспрессией MUC1.
Иммунное взаимодействие клеток в желчных протоках у кошек с лимфоцитарным холангитом, аналогично наблюдаемому у людей с первичным склерозирующим холангитом(PSC). PSC характеризуется прогрессирующим воспалением, фиброзом и разрушением внутри- и внепечёночных желчных протоков, в результате развивается билиарный фиброз, цирроз, приводящий к печёночной недостаточности.
PSC это комплексное заболевание, основанное на генетике, врождённом и адаптивном иммунитете и влиянии окружающей среды. Часто это связано с ВЗК и предполагает иммунную атаку против клеток желчевыводящего тракта и может вызывать хоуминг лимфоцитов памяти, количество которых повышается, как последствия ВЗК для печени. Обнаружением молекулы клеточной адгезии (MAdCAM-1) и хемокинов (C-C motif) лиганда (CCL25), местом локализации которых считался только кишечник, которые активируются в печени в условиях воспаления, поддерживается общая концепция, что этот механизм может привлекать лимфоциты в поражённую печень и кишечник. Экспрессия MadCAM-1 так же может вызвать лимфоцитарное воспаление островковых клеток при сахарном диабете, но это не всегда связано с иммуно-опосредованным панкреатитом. Разнообразные антигены могут быть вовлечены в PSC. В последнее время идентификация B-тубулина изотипа 5 (TBB5), который имеет высокое соответствие с бактериальным белком деления клеток FtsZ, как антинейтрофильное цитоплазматическое аутоантитело (ANCA), предполагает, что иммунные ответ на миграцию бактерий возможен при наличии нарушений порозности слизистой кишечника, что способствует воспалению у восприимчивого человека. В то время как PSC способствует аутоиммунному панкреатиту, всё чаще считают, что нарушение проходимости желчевыводящих путей относятся к подтипу PSC, холангиту, ассоциированному с иммуноглобулином (Ig) G4. Эта болезнь, связана с увеличением сывороточного IgG4/IgE, обильной инфильтрацией IgG4-positive плазмацитарных клеток и лимфоцитов, аутоантигенов и стероидной восприимчивости. Считается, что аутоантигены, аутоантитела (такие как лактоферрин, карбоангидразы) и потенциальные патогены могут управлять IgG4-опосредованным воспалением, но это ещё предстоит определить. Ряд других органов также может быть вовлечён в этот процесс: слюнные железы (Sjögren’s syndrome), стриктуры желчевыводящих путей, узелки в лёгких, аутоиммунный тиреоидит, интерстициальный нефрит (обусловленный инфильтрацией IgG4-positive плазматических клеток и осаждением IgG4 на тубулярной базальной мембране). Примечательно, что нефрит, который считают сопутствующей возрастной патологией, часто диагностируют у кошек с холангитами и/или панкреатитами.
Лечение триадитов
Термин триадит применяется к синдрому, который охватывает спектр воспалительных заболеваний печени, поджелудочной железы и кишечника, поэтому, для выбора тактики лечения, требуется особо тщательная оценка общего состояния здоровья пациента и определение конкретного типа, и степени тяжести изменений в каждом из этих органов. Лекарственные препараты для лечения каждого из заболеваний необходимо рассматривать комплексно, для того, чтобы оценить возможность негативных последствий при их одновременном применении, поэтому необходим индивидуальный подход к каждому пациенту.
Приоритеты в лечении у кошек с триадитами
Лечение триадитов начинают с получения результатов клинического осмотра, клиникопатологических тестов, которые направлены на дифференциацию заболевания (цитология тканей печени, поджелудочной железы, мезентериальных лимфатических узлов, культуральные исследования желчи). У кошек с персистирующей рвотой, абдоминальной болью, желтухой, анорексией, гиповолемией, признаками шока, сепсиса, гипотермии или лихорадки, первичная цель лечения — это поддержание общего состояния и поиск возможных причин заболевания. Симптоматическое лечение включает в себя инфузионную терапию, обезболивание, противорвотные средства и антибиотики (при подозрении на сепсис, наличии нейтрофилии с левым сдвигом) (таб. 3). Животным с анорексией назначают энтеральное питание (жидкие корма через назо-фарингеальные зонды). У кошек с подтверждённым триадитом основное лечение направлено на более поражённый орган. Например: острый панкреатит, с подозрением на холангит, холецистит, обструкцию билиарного тракта и возможную перфорацию кишечника. В этом случае необходимо определить необходимость немедленного хирургического вмешательства.
Дифференциальная диагностика триадита основана на оценке гистопатологического материала каждого органа и выявлении бактериальной инфекции в них (культуральные исследования желчи и тканей печени, и FISH — исследование печени и поджелудочной железы), для чего проводится диагностическая лапаротомия. Это также хорошая возможность для установки эзофагостомической трубки. Если диагностическая лапаротомия невозможна или нецелесообразна, проводят минимально инвазивные исследования, такие как эндоскопия и тонкоигольна биопсия участков поражённых органов под контролем УЗИ. Последующая терапия основана на основании наличия бактериальной инфекции в билиарном тракте, поджелудочной железе или кишечнике (нейтрофильный или гранулематозный энтерит) с определением чувствительности этой микрофлоры к антибактериальным препаратам (таб. 3.).
Таблица 3. Лечение триадита: панкреатиты, воспалительные заболевания печени и кишечника
Гемобартонеллез - довольно распространенное кровепаразитарное заболевание кошек, вызываемое Haemobartonella felis. Его нельзя отнести полностью ни к микоплазмам, ни к риккетсиям, так как он занимает промежуточное положение между ними, по последним данным его больше относят к микоплазмам.
Паразит проникает в цитоплазматическую мембрану эритроцита, повреждает ее сокращая его жизнь. В дальнейшем такой поврежденный эритроцит лизируется в клетках селезенки и печени. Локализация гемобартонеллез происходит и на поверхности тромбоцитов, лейкоцитов, а также в плазме. Размножение паразита происходит в органах ретикулоэндотелиальной системы - печени, селезенки, лимфатических узлах и костном мозге. Организм, вырабатывая антитела и аутоантитела на собственные эритроциты может формировать и их аутоиммунный ответ против и незараженных эритроцитов. Таким образом, происходит иммуноопосредованный внутрисосудистый гемолиз с последующим разрушением эритроцитов системой комплемента.
В результате, когда гибель эритроцитов преобладает над работой системы гепомоэза, развивается анемия, в результате недостаточного питания и кислородоснабжения функции органов нарушаются, происходит дистрофия клеток паренхиматозных органов, нарушается обмен веществ и кислотно-основное равновесие, развивается ацидоз. Особенно тяжело заболевание протекает у животных со сниженным иммунным статусом или у животных прошедших спленэктомию. Так в последнем случае, гемобартонеллез может встречаться у собак, а среди кошек он чаще встречается при наличии вирусного лейкоза или иммунодефицита. Гемобартонеллез может длительно протекать латентно, активация гемопаразита происходит, как правило, при наличии при этом при наличии системных патологий, влияющих на гемопоэз и иммунную систему, такие как хронические болезни почек, системные воспалительные реакции, вирусные инфекции и т.д. Кроме того, гемопаразит активизируется при стрессе, оперативных вмешательствах, родах, лактации и даже вакцинации. Гемобартонеллез часто выявляется и у клинически здоровых животных, причем степень анемии и паразитемии не коррелируют друг с другом.
Данный кровепаразит не может существовать вне организма, поэтому заражение может происходить только при контакте с зараженным животным, в том числе при укусе во время драки или посредством укуса блох или клещей и даже комаров. Соответственно пик заболеваемости приходится на осенне-летний период. Конечно, заражение происходит и при переливании донорской крови у непроверенного животного, в возможно также заражение при оперативных вмешательствах при использовании плохо промытых хирургических инструментов. Может быть передача гемобартонелл от матери к котятам, но на какой именно стадии (трансплацентарно, при родах или лактации) не известно. В целом, животные носители, т.е. не имеющие клинической симптоматики способны заражать других кошек, по крайне мере, в течение не менее 6 месяцев.
При выявлении анемии необходимо исключать все причины, приводящие к ней. Например, отравления крысиным ядом, антисептиками (как метиленовым синим), гликозидами (Сапонинами), Фенотиазном, нафталином, тяжелыми металлами (например, свинцом). К анемии может приводить и окислительное повреждение эритроцитов, как например, при приеме Парацетамола или регулярном потреблении лука или капусты. Анемия может развиваться и при нарушении метаболизма (например, порфинурия у кошек и жировой липидоз печени), а также при наличии гельминтоза и других кишечных паразитов и при иммуно-опосредованной анемии.
Инкубационный период может длиться от 8 до 17 и даже 20 дней. Более предрасположены к данному заболеванию молодые коты, особенно, в возрасте от одного до трех лет, к которых заболевание протекает в острой и довольно тяжелой форме. В целом, можно выделить следующие стадии развития данного заболевания: инкубационный, острая стадия, стадия выздоровления и носительства.
После выздоровления они, однако, часто остаются носителями. У кошек же чаще хроническая форма, протекающая менее выраженно и в течение длительного времени, так стадия бессимптомного носительства может быть несколько лет или даже в течение всей жизни. Ее обострение может произойти при любым условиях, снижающих резистентность организма, как например, инфекционное или онкологическое заболевание, хирургическое вмешательство, неполноценное питание и содержание, стресс и т.п. Заболевание может иметь бессимптомную форму. Однако, при этой форме паразит активизируется в период беременности, что приводит к абортам. Собаки также могут заражаться данным паразитом, однако, он не вызывает у них клинической симптоматики заболевания. Клинические проявления гемобартонеллеза встречаются не столь часто, по статистике только у 25% носителей. Их проявление будет зависеть от множества факторов, в т. ч. от патогенности штамма возбудителя и состояния иммунной системы животного.
Так как заболевание вызывает анемию, то у животного будут наблюдаться соответствующие симптомы: бледность внешних слизистых оболочек, вялость, апатия, малоподвижность, сонливость, тахикардия, тахипноэ, снижение аппетита, парарексия, истощение, увеличение внешних лимфатических узлов, хрипота голоса, гипотрихоз, воспаление, алопеции, шелушение, в виду сухости кожи, вплоть до дерматитов и диатезных геморрагий. При уже тяжелой форме течения и развития полиорганной недостаточности повышенный распад эритроцитов ведет к накоплению гемоглобина в печени, что вызывает ее воспаление, что дает соответствующий симптом - иктеричность кожи и внешних слизистых оболочек и микроглобинурию. Иногда при остром течение возможна и лихорадка, что говорит о сильнейшей интоксикации, вследствие острой формы, подсоединения вторичной инфекции или развития воспаления, например, при орхите. При острой форме симптомы более выраженные и тяжелые, при хронической, напротив, малозаметные, медленно прогрессирующие во времени.
Для постановки диагноза необходимы специфические тесты. Гемобартонеллу иногда можно выявить и в ходе световой микроскопии, посредством окрашивания мазка периферической крови по Романовскому-Гимзе или с помощью акридин оранжевого или Грюнвальд-Гимза или Райта и Райта-Гимза. При этом данный гемопаразит можно обнаружить не только на поверхности мембран эритроцитов, но также лейкоцитов, тромбоцитов и даже в плазме крови. Однако, этот последний метод не всегда надежен, в виду быстрого оседания раствора и краткости жизни паразита. Так только где-то у 25% зараженных животных будет выявлен данный паразит. Кроме того, гемобартонелла не на всех стадиях своего развития присутствует в эритроцитах, поэтому данную диагностику необходимо повторять заново через несколько дней. Кроме того, к примеру, в первый день заболевания данный паразит чаще не может быть обнаружен в крови. В целом, есть много факторов, в виду которых данный метод диагностики может давать как ложноположительные (например, в случае возникновения артефакта при неправильной сушке или фиксации мазка, а также гемобартонеллез можно спутать с седиментом краски) так и ложноотрицательные результаты (в связи с отсутствием паразита в крови в течение первых часов болезни или в связи с циклической паразитемии, кроме того высокая концентрация стабилизатора ЭДТА может приводить к отщеплению гемопаразита от поверхности эритроцита).
По количеству пораженных эритроцитов можно иногда судить о степени тяжести заболевания. Так клинически значимым является поражение более 10% эритроцитов. Данный метод необходимо подтверждать ПЦР диагностикой. Это самый чувствительный специфический метод, в настоящий момент - метод выбора, обнаруживающий фрагменты ДНК возбудителя, позволяющий выявлять гемобартонеллез еще на стадии носительства или уже спустя 8 дней после заражения, однако, важно его применение еще до начала антибиотикотерапии. Считается, что ПЦР диагностика гемобартонеллеза на 37% более эффективна, чем микроскопия мазка крови. Однако, данные по ПЦР диагностики следует интерпретировать и с учетом клинической симптоматики. При отрицательном результате по ПЦР, с большей вероятностью считается, что данное заболевание отсутствует у животного. ПЦР диагностику при положительном результате желательно проводить потом еще раз повторно где-то через полгода после окончания курса лечения, чтобы убедиться в выздоровлении животного.
Возможно также использование метода меченных антител - иммунофлюоресценции антител к возбудителю (метод РИФ), данный метод более надежен, чем микроскопия.
Гемобартенеллез часто сопровождает хронические вирусные инфекции кошек, поэтому при его выявлении необходимо проводить также исследования и на другие причины анемии - вирусный лейкоз кошек и вирусный иммунодефицит кошек.
Обязательным в ходе диагностики является общеклинический анализ крови. Примечательным показателем гемобартонеллеза является регенеративная анемия (повышенное количество ретикулоцитов), если она не осложнена, к примеру, хронической вирусной инфекцией или выраженной почечной недостаточностью. Анемия макроцитарная, полихроматофильная, гипохромная или нормохромная, часто наблюдаются анизоцитоз, микроцитоз, полихромазия, эритроциты с базофильной зернистостью и тельцами Жолли или Гейнца, а также нормобласты.
Соответственно, наблюдается гемоглобинемия и, как правило, тромбоцитопения, лейкоцитоз, но возможна и лейкопения, повышение СОЭ и нормобластов. В плазме крови может развиваться билирубинемия. При сильном гемолизе эритроцитов в моче развивается гемоглобинурия, цвет мочи темнеет.
В результате нарушения функции печени может развиваться, как правило, незначительная гемоглобинурия, что можно увидеть в анализах мочи наличием уробилиногена и гемоглобина, что визуально дает темный цвет мочи.
При ультразвуковой диагностике гемобартонеллеза, как правило, выявляется гепатомегалия и спленомегалия, селезенка при этом заболевании испытывает сильнейшие нагрузки в виду гибели большого количества эритроцитов, которые данный орган должен вывести.
Гемобартенеллез лечится специфическими антибиотиками тетрациклинового ряда. Это прежде всего антибиотики тетрациклинового ряда (Доксициклин, Окситетрациклин). Так Доксициклин применяют в дозе 10 мг/кг/сут. (от 5 мг/кг/сут.) на протяжении 2 и даже 4 недель, однако, даже при таком длительном курсе может не быть полной элиминации возбудителя.
При непереносимости Доксициклина альтернативой лечения являются фторхинолоны. Это прежде всего Энрофлоксацин в дозе 5 мг\кг в сутки курсом около 10 дней. Однако, часто Энрофлоксацин даже в дозе 10 мг/кг в течении 2 недель может не дать достаточного эффекта, а у данного препарата больше побочных действий. Более высокие дозы могут привести к потере зрения. Его нельзя назначать беременным и до годовалого возраста. У щенков и котят может быть его непереносимость в виде рвоты, а также на месте его инъекции может развиваться некроз кожи. Однако, Доксициклин также не рекомендуется котятам и щенкам по причине его накопления в костной ткани, что в дальнейшем нарушает формирование костной системы и зубов. Из других побочных эффектов Доксициклин обладает гепатотоксичностью, а при длительном применении - местно-раздражающим действием при инъекционной форме применения. Поэтому котят и щенков пробуют лечить антипротозойными препаратами, как Имидокарб, при этом достаточно одной инъекции. Однако, эти препараты помогают только при медленном течении болезни. Если дней через 5 наблюдается положительная динамики в общеклиническом анализе крови, то эффект от препарата считается достигнутым. Возможно также применение противопротозойного препарата Азидина в дозе 3,5 мг/кг. В дозе 5 мг/кг/сут. 2-4 недели он элиминирует всех возбудителей.
Азитромицин, применяемый при лечении микоплазмоза у людей, не эффективен при лечении гемобартенеллеза.
Возможно также применение антибиотиков левомецитинового ряда в дозе 25-50 мг в 2-3 приема на протяжении около 2-3 недель, однако, он также не вызывает полной элиминации возбудителя.
Для лечения истощенных и ослабленных кошек можно использовать Тиметосул (в составе которого Сульфадиазин и Триметоприм) в парентеральной форме. Он используется всего лишь трехкратно в дозе 16 и 32 мг/кг.
Необходимо также и симптоматическое лечение. Назначаются препараты железа и витамины группы В. Для поддержки печени необходимы гепатопротекторы (как, например, Гептрал). В случае выраженной анемии (при гематокрите от 20) необходимо уже переливание цельной крови или эритроцитарной массы. При отсутствии хронический вирусных инфекций хороший эффект дают стимуляторы эритропоэза (как Эпокрин, Дарбопоэтин и т.д.). При наличии же вирусного лейкоза кошек прогноз становится, особенно, неблагоприятным. При выраженной тромбоцитопении, в целях предотвращения аутоиммунного разрушения эритроцитов, т.е. для подавления эритрофагоцитоза и снижения вторичной иммуноопосредованной гемолитической анемии (т.е. когда наблюдается прогрессирующая анемия) необходимы кортикостероиды в иммуносупрессивной дозе, т.е. от 2 мг/кг/сут. с последующим ее плавном снижении. При сниженном аппетите необходимо принудительное кормление или даже зондовое с помощью эзофагостомы. Диета в стадию восстановления должна быть высокобелковой, богатой витаминами и минералами. При выраженном обезвоживании проводится гидратация для восстановления водно-электролитного баланса. Без лечения смертность обычно достигает около 30%. После лечения кошки, как правило, остаются носителями гемобартонелл, но рецидивы встречаются крайне редко.
Для профилактики заражения кошек гемобартонеллезом необходимо исключать их контакт с бездомными животными и использовать репелленты и акарициды в виде ошейников и препаратов топикального применения. Важна и периодическая дезинсекция мест обитания бездомных кошек. Необходимо следить за полноценным кормлением и содержанием животного. Вакцина от гемобартонеллеза пока еще не разработана.
Параанальные железы у кошки представляют собой парные железы внешней секреции, расположенные с обеих сторон от анального отверстия. Внутренняя оболочка «мешочков» содержит большое количество сальных и апокриновых желез. Секрет, который продуцируют параанальные железы, имеет густой вид кремового, белого, а иногда светло-серого цвета .
В экссудате содержаться феромоны - пахучие летучие вещества, обладающие острым неприятным запахом. Данные выделения используются кошками для того, чтобы метить свою территорию, привлекать партнеров в период спаривания, распознавать чужаков.
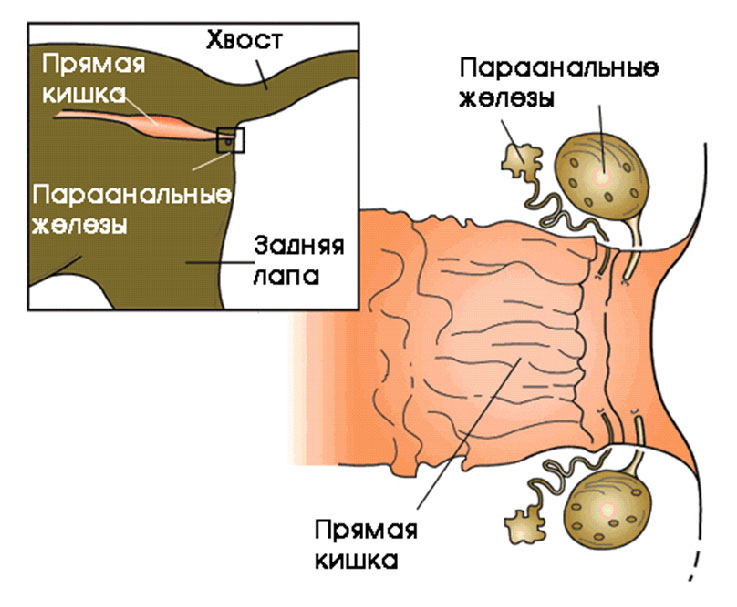
Секрет из параанальных желез выделяется кошкой в незначительном количестве в результате мышечных сокращений и перистальтики кишечника через небольшой канал. Естественным путем освобождение «мешочка» происходит в процессе дефекации или во время «распрыскивания» секрета во время обороны, при нанесении территориальных меток.
Выделяемый секрет у кошки делает хвостовую часть вокруг ануса более жирной, облегчая процесс дефекации.
При воспалении параанальных желез у кошки происходит застой образуемого железами секрета, в запущенных случаях возникает абсцесс и образуется свищ.
Причины, вызывающие у кошки воспаление параанальных желез.
Современные кошки, проживая в комфортных домашних условиях, когда у них отсутствует необходимость использовать параанальные железы для защиты от потенциальных противников привело к тому, что они утратили природную способность очищать свои параанальные железы.
Воспаление желез у кошки возникает в результате влияния ряда факторов:
- Хронические заболевания органов пищеварения, которые сопровождаются запорами (запор у кошки) и постоянной диареей (понос у кошки).
- Генетическая предрасположенность.
- Системные инфекционные заболевания (хламидиоз кошек, панлейкопения кошек, лептоспироз и др.).
- Паразитарные заболевания (глисты у кошек).
- Гиподинамия, малоподвижный образ жизни в условиях городской квартиры.
- Ожирение (диагностика ожирения).
- Травмы анальной области.
- Врожденная узость выводных каналов желез.
- Кормление жидкой пищей, костями.
- Беременность (беременность у кошки).
Патогенез. Механизм развития воспаления параанальных желез у кошки выглядит следующим образом:
Сначала происходит нарушение выведения секрета из желез, в результате чего в железах скапливается большое количество секрета. Происходит уплотнение образованного секрета, что еще больше препятствует его выделению при дефекации у кошки. Из кала в железы попадает условно — патогенная микрофлора, которая приобретает повышенную вирулентность и начинает быстро размножаться. Секрет становится густым, приобретает темно-коричневый цвет и зловонный запах. Если своевременно не будет начато лечение, то на месте железы появляется абсцесс. При «созревании» абсцесса его гнойные массы приводят к разрыву оболочки железы и получаем абсцедирующий абсцесс. Данный абсцесс в дальнейшем переходит в незаживающие свищи с выходом в просвет прямой кишки или с выходом в прианальную зону.
Во время всего процесса воспаления пара анальных желез кошка испытывает боль и зуд в области анального отверстия.
Клиническая картина. Заболевание у кошки сопровождается воспалением в преанальной области. Кошка постоянно вылизывает область хвоста и анального отверстия, при движении хвост плотно прижат к анусу. Из за болезненности кошка старается меньше двигаться, отказывается от активных игр, старается больше лежать, нарушается походка. При поглаживании в области хвоста реагирует болезненно, проявляет признаки агрессии. С целью освобождения накопившегося в железах секрета «ездит» на пятой точке по полу. Хвост у кошки приобретает сальный вид. В запушенных случаях регистрируем повышение температуры тела.
Ветеринарные специалисты при осмотре анальной области отмечают — припухлость, отек и покраснение тканей вокруг анального отверстия. При надавливании на параанальные железы из анального отверстия выделяется неприятного цвета маслянистый экссудат бурого цвета.
Диагноз на воспалении параанальных желез ветеринарный специалист ставит во время клинического осмотра больной кошки путем визуального осмотра анальной области и оценки количества и характера секрета. При помощи салфетки врач сдавливает параанальные железы кошки и проводит исследование выделившегося секрета - цвет, консистенция, количество. При необходимости секрет направляют в ветеринарную лабораторию на посев для определения вида патогенной микрофлоры и на подтитровку к антибиотикам.
Лечение. Основу лечения заболевания у кошек является механическое освобождение параанальных желез от скопившегося экссудата. Данную процедуру можно проводить несколькими методами. В том случае, когда секрет в железах жидкий и не затвердел, то их очистку можно провести наружным путем.
Для этого специалист проведя дезинфекцию рук надевает хирургические перчатки и стерильными марлевыми тампонами с помощью большого и указательного пальцев надавливает на параанальные железы.
При наличии в параанальных синусах густого и вязкого содержимого ветеринарные специалисты применяют внутренний метод освобождения содержимого параанальных желез. При этом методе в стерильных перчатках указательный палец вводится кошке в анус. Большой палец снаружи массажирует железу с целью стимулирования отхождения секрета. В дальнейшем ветеринарный специалист с помощью катетера проводит их промывание антисептическими растворами. При наличии показаний больной кошке назначаются антибактериальные препараты (свечи с противовоспалительным действием). В зависимости от тяжести воспаления манипуляцию необходимо повторить 2-3 раза до полного очищения мешочков. При частых рецидивах заболевания рекомендуется операция по удалению параанальных желез.
Профилактика заболевания основана на предупреждении развития воспаления параанальных желез. С этой целью владельцы кошки должны:
Лейкоцитарные отряды
Для людей «непосвященных», общий анализ крови с лейкоцитарной формулой (1.0.D2.202) чаще всего похож на «китайский язык». Найти «предложение» о природе воспаления, в котором, на первый взгляд, кажется совершенно невозможным. Тогда как на самом деле, для первичного выяснения характера инфекции, чаще достаточно и «беглой» оценки численности различных представителей лейкоцитов.
1. Нейтрофилы
«Группой моментального реагирования» в борьбе с бактериями являются нейтрофилы, относительное (в %, по отношению к другим разновидностям лейкоцитов) повышение которых в общем анализе крови является надежным маркером любого бактериального воспаления и, соответственно, обоснованием в пользу антибактериального характера лечения.
Тогда как абсолютное увеличение численности нейтрофилов (клеток на литр крови) – чаще сопровождает достаточно тяжелые формы инфекций.
Эти представители лейкоцитов самыми первыми мигрируют из крови в очаг воспаления, где буквально «поедают» и «переваривают» врага с помощью «ядовитых» гранул.
Правда после такого «перекуса», нейтрофилы и сами оказываются нежизнеспособны и погибают. А клиническим отражением этого процесса является образование гноя в очаге воспаления.
2. Лимфоциты
Одновременно с увеличением нейтрофилов, в крови «бактериального» больного наблюдается относительное (в %) снижение основных борцов с вирусами – лимфоцитов, что является отражением нормального перераспределения «иммунных активов» под текущие задачи защиты. А сам процесс имеет название «относительной лимфопении».
3. Моноциты
В качестве «ликвидаторов последствий» воспаления, в очаг из крови «стягиваются» моноциты. Которые уже «на месте» трансформируются в более крупные – макрофаги, и эффективно очищают «пространство» от разрушенных клеток и бактерий.
Максимальное повышение моноцитов в общем анализе крови обычно наблюдается только в самом конце воспаления, как маркер завершения процесса и начала периода восстановления.
А, помимо прочего, моноциты - «солдаты» универсального назначения, и задействованы как при бактериальном, так и вирусном (особенно герпетического происхождения), а также аутоиммунном и некоторых других механизмах воспаления. Поэтому их повышение в той или иной степени характерно практически для всех видов воспалительного процесса.
Нейтрофильное воспаление у кошек сопровождает любую бактериальную или грибковую инфекцию. Белые клетки крови уничтожают чужеродные частицы, однако при этом происходит массовая гибель нейтрофилов в очаге поражения.
Читайте также:
- Можно ли размачивать сухой корм для кошек и котят и как это делать правильно
- Осенняя прохлада и ваша кошка: о чем следует помнить
- Возрастные изменения поведения у кошки
- Какие антибиотики можно давать кошкам при инфекциях и гнойных ранах
- Стресс у кошки после стрижки: почему животное ведет себя странно и не может лечь?

