Гемоторакс: этиология, патогенез, клиническая картина, диагноз, лечение, профилактика
Обновлено: 05.10.2024
ГЕМОТОРАКС (haemothorax; греч. haima кровь + thorax грудь; син. гематоторакс)— скопление крови в плевральной полости.
Описание Г. как осложнения ранения груди встречаются уже у врачей средневековья — Парацельса, А. Паре. Первые научно обоснованные рекомендации по лечению Г. принадлежат Н. И. Пирогову. До конца 19 в. существовала тактика лечения Г. поздними (на 3—5-й день после ранения) пункциями. В 1916 г. на XIV съезде русских хирургов многие хирурги (в частности, Л. Г. Стуккей) выступили за активную тактику при открытых ранениях груди, в т. ч. и при Г. Однако ранние плевральные пункции при Г. начали применять лишь во время боевых действий на р. Халхин-Гол (М. Н. Ахутпин, А. А. Вишневский). Современные принципы лечения Г. были разработаны во время Великой Отечественной войны В.-И. Колесовым, П. А. Куприяновым, В. С. Левитом и др.
Общие сведения
Гемоторакс является вторым по частоте (после пневмоторакса) осложнением травм грудной клетки и встречается у 25 % больных с торакальной травмой. Довольно часто в клинической практике наблюдается комбинированная патология - гемопневмоторакс. Опасность гемоторакса заключается как в нарастающей дыхательной недостаточности, обусловленной сдавлением легкого, так и в развитии геморрагического шока вследствие острого внутреннего кровотечения. В пульмонологии и торакальной хирургии гемотракс расценивается как неотложное состояние, требующее оказания экстренной специализированной помощи.
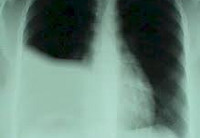
Симптомы гемоторакса
Клиническая симптоматика гемоторакса зависит от степени кровотечения, сдавления легочной ткани и смещения органов средостения. При малом гемотораксе клинические проявления выражены минимально или отсутствуют. Основными жалобами служат боли в грудной клетке, усиливающиеся при кашле, умеренная одышка.
При гемотораксе среднего или большого размера развиваются дыхательные и сердечно-сосудистые расстройства, выраженные в различной степени. Характерна резкая боль в груди, иррадиирующая в плечо и спину при дыхании и кашле; общая слабость, тахипноэ, снижение АД. Даже при незначительной физической нагрузке происходит усиление симптоматики. Больной обычно принимает вынужденное сидячее или полусидячее положение.
При тяжелом гемотораксе на первый план выступает клиника внутриплеврального кровотечения: слабость и головокружение, холодный липкий пот, тахикардия и гипотония, бледность кожных покровов с цианотичным оттенком, мелькание мушек перед глазами, обмороки.
Гемоторакс, сопряженный с переломом ребер, как правило, сопровождается подкожной эмфиземой, гематомами мягких тканей, деформацией, патологической подвижностью и крепитацией отломков ребер. При гемотораксе, протекающем с разрывом легочной паренхимы, может возникать кровохарканье.
В 3-12% случаев формируется свернувшийся гемоторакс, при котором в полости плевры образуются кровяные сгустки, фибринные наслоения и шварты, ограничивающие дыхательную функцию легкого, вызывая развитие склеротических процессов в легочной ткани. Клиника свернувшегося гемоторакса характеризуется тяжестью и болью в грудной клетке, одышкой. При инфицированном гемотораксе (эмпиеме плевры) на первый план выходят признаки тяжелого воспаления и интоксикации: лихорадка, ознобы, вялость и др.
Патогенез
Скопление крови в полости плевры вызывает компрессию легкого на стороне поражения и смещение органов средостения в противоположную сторону. Это сопровождается уменьшением дыхательной поверхности легкого, возникновением расстройств дыхания и гемодинамики. Поэтому при гемотраксе нередко развивается клиника геморрагического и кардио-пульмонального шока с острой дыхательной и сердечной недостаточностью.
Уже в ближайшие часы после попадания крови в плевральную полость развивается асептическое воспаление плевры - гемоплеврит, обусловленный реакцией плевральных листков. При гемотораксе возникает отек и умеренная лейкоцитарная инфильтрация плевры, набухание и слущивание клеток мезотелия. В начальном периоде излившаяся в плевральную полость кровь практически не отличается по составу от периферической крови. В дальнейшем в ней происходит снижение гемоглобина, уменьшение эритроцитарно-лейкоцитарного индекса.
Попадая в плевральную полость, кровь вначале сворачивается. Однако затем вскоре наступает процесс фибринолиза, и происходит повторное разжижение крови. Этому способствуют антикоагулянтные факторы, содержащиеся в самой крови и плевральной жидкости, а также механическое дефибринирование крови за счет дыхательной экскурсии грудной клетки. По мере истощения механизмов антикоагуляции происходит свертывание крови и формирование свернувшегося гемоторакса. В случае присоединения микробного инфицирования на фоне гемоторакса довольно быстро может возникать эмпиема плевры.
Клиническая картина
Клиническая картина зависит от степени выраженности кровотечения, сдавления и повреждения легкого и смещения средостения.
Состояние раненых и больных с большим Г. тяжелое. Отмечается беспокойство, одышка, боли в груди, кашель, иногда с кровохарканьем, реже легочное кровотечение, бледность и цианоз кожи, учащение пульса, понижение АД. Положение больного чаще полусидячее.
При среднем Г. состояние раненых и больных менее тяжелое, однако отмечаются бледность, тахикардия, одышка, даже незначительная физ. нагрузка вызывает у них усиление этих симптомов.
Состояние раненых и больных с малым Г. может быть относительно удовлетворительным. Боли, редкий кашель и умеренная одышка могут самостоятельно исчезнуть в течение нескольких дней.
При осмотре отмечают отставание пораженной половины грудной клетки при дыхании. Голосовое дрожание ослаблено, отмечается притупление перкуторного звука, смещение средостения, ограничение подвижности нижнего легочного края, степень которых зависит от количества крови в плевральной полости. Иногда выявляется симптом Бирмера — изменение звука при перкуссии грудной клетки в зависимости от положения тела больного за счет свободного перемещения излившейся крови в плевральной полости; в положении сидя звук более низкий, чем в положении лежа.
Инфицирование Г. приводит к ухудшению общего состояния больного. Появляются апатия, вялость, тахикардия, повышение температуры тела и другие признаки эмпиемы плевры (см. Плеврит, гнойный) .
Диагноз основывается на данных анамнеза, клин.-рентгенол, исследования и результатах плевральных пункций. О величине кровопотери судят по различным пробам, применяющимся в клин, практике (см. Кровопотеря).
Аспирация крови из плевральной полости при пункции — достоверный диагностический признак Г. Определенные диагностические трудности возникают при свернувшемся Г., когда при плевральной пункции удается получить только небольшое количество темной крови. Стерильный и инфицированный Г. можно дифференцировать по характеру пунктата, используя простую и достаточно достоверную пробу H. Н. Петрова. Полученную при пункции кровь разводят дист, водой в 5 раз — при отсутствии инфекции после гемолиза жидкость остается прозрачной, при наличии инфекции она мутнеет. Определенную диагностическую ценность имеет бактериол, и цитол. исследование пунктата. Судить о прекращении кровотечения в плевральную полость можно с помощью пробы Рувилуа — Грегуара: если полученная при плевральной пункции кровь свертывается в шприце или пробирке — кровотечение продолжается, если кровь не свертывается — кровотечение прекратилось или продолжается крайне медленно.
Для рентгенодиагностики Г. применяют Полипозиционное исследование (см.). В вертикальном положении исследуемого небольшое количество крови может скапливаться в наддиафрагмальном пространстве, создавая ошибочное представление о высоком стоянии купола диафрагмы и ограничении ее подвижности. Придание больному горизонтального положения вызывает либо растекание крови по задней поверхности легкого, что проявится равномерным понижением прозрачности соответствующего легочного поля, либо затекание жидкости в парамедиастинальное пространство и симптом расширения тени средостения. Скопление небольших количеств крови только в заднем плевральном синусе удается выявить при латероскопии.
Если Г. достигает 200—300 мл, появляется понижение прозрачности легочного поля треугольной формы, сливающееся с диафрагмой и характерной косой верхней границей. Скопление большого количества крови сопровождается смещением средостения в противоположную сторону. Появление воздуха в плевральной полости при Г. (гемопневмоторакс) определяется по наличию горизонтального уровня жидкости и воздуха над ним.
Причины гемоторакса
Выделяют три группы причин, наиболее часто приводящих к развитию гемоторакса: травматические, патологические и ятрогенные.
- Под травматическими причинами понимают проникающие ранения или закрытые повреждения грудной клетки. К торакальной травме, сопровождающейся развитием гемоторакса, относятся ДТП, огнестрельные и ножевые ранения грудной клетки, переломы ребер, падения с высоты и др. При подобных травмах довольно часто происходит повреждение органов грудной полости (сердца, легких, диафрагмы), органов брюшной полости (травмы печени, селезенки), межреберных сосудов, внутренней грудной артерии, внутригрудных ветвей аорты, кровь из которых изливается в плевральную полость.
- К причинам гемоторакса патологического характера причисляют различные заболевания: рак легкого или плевры, аневризму аорты, туберкулез легких, абсцесс легкого, новообразования средостения и грудной стенки, геморрагический диатез, коагулопатии и др.
- Ятрогенными факторами, приводящими к развитию гемоторакса, выступают осложнения операций на легких и плевре, торакоцентеза, дренирования плевральной полости, катетеризации центральных вен.
Классификация
В зависимости от количества излившейся в плевральную полость крови различают малый, средний и большой (тотальный) Г. При малом Г. кровь чаще занимает только синусы плевральной полости, при среднем Г. достигает угла лопатки; при большом (тотальном) Г.— занимает всю или почти всю плевральную полость.
Кроме того, выделяют ограниченный Г. (обычно малый), при к-ром излившаяся кровь за счет плевральных спаек или быстрого свертывания скапливается в отдельных участках плевральной полости; в зависимости от локализации различают верхушечный, междолевой, поддиафрагмальный, паракостальный, парами диастинальный Г.
Различают Г. с прекратившимся или продолжающимся кровотечением. В зависимости от наличия или отсутствия инфекции в плевральной полости говорят об инфицированном (пиогемоторакс) или неинфицированном Г. При свертывании крови, излившейся В плевральную полость, Г. называют свернувшимся. Г. может быть закрытым или открытым; при одновременном наличии в плевральной полости воздуха и крови речь идет о гемопневмотораксе.
Диагностика
Для постановки диагноза уточняются подробности истории заболевания, проводится физикальное, инструментальное и лабораторное обследование. При гемотораксе определяется отставание пораженной стороны грудной клетки при дыхании, притупление перкуторного звука над уровнем жидкости, ослабление дыхания и голосового дрожания. При рентгеноскопии и обзорной рентгенографии легких выявляется коллабирование легкого, наличие горизонтального уровня жидкости или сгустков в полости плевры, флотация (смещение) тени средостения в здоровую сторону.
С диагностической целью выполняется пункция плевральной полости: получение крови достоверно свидетельствует о гемотораксе. Для дифференциации стерильного и инфицированного гемоторакса проводят пробы Петрова и Эфендиева с оценкой прозрачности и осадка аспирата. С целью суждения о прекращении или продолжении внутриплеврального кровотечения выполняют пробу Рувилуа-Грегуара: свертывание полученной крови в пробирке или шприце свидетельствует о продолжающемся кровотечении, отсутствие коагуляции говорит о прекращении кровотечения. Образцы пунктата направляют в лабораторию для определения гемоглобина и проведения бактериологического исследования.
При банальном и свернувшемся гемотораксе прибегают к лабораторному определению Нb, количества эритроцитов, тромбоцитов, исследованию коагулограммы. Дополнительная инструментальная диагностика при гемотораксе может включать УЗИ плевральной полости, рентгенографию ребер, КТ грудной клетки, диагностическую торакоскопию.
Прогноз
Прогноз при неосложненном Г. благоприятней. При инфицированном и свернувшемся Г. он более серьезен вследствие большой вероятности развития эмпиемы плевры.
Лечение
Малый стерильный Г. может самостоятельно рассосаться без каких-либо леч. мероприятий. Рассасывание Г. происходит медленно, в течение 1—2 мес. По мере рассасывания кровь в плевральной полости постепенно «разбавляется» экссудатом и содержимое плевральной полости становится серозным. У большинства больных после ликвидации Г. остаются плевральные сращения.
В большинстве случаев лечение малого и среднего Г. без признаков продолжающегося кровотечения и присоединившейся инфекции осуществляется плевральными пункция ми наряду с медикаментозным лечением., Плевральные пункции (см.) проводят по общепринятой методике, по возможности удаляют всю кровь из полости.
Инфицированный или свернувшийся Г. в большинстве случаев приводит к возникновению эмпиемы плевры. Поэтому во всех случаях кровь и воспалительный экссудат следует максимально удалять из плевральной полости сразу после установления диагноза Г. или гемоплеврита. Свернувшийся Г. является показанием к торакотомии (см.), удалению сгустков крови и дренированию плевральной полости.
Большой Г., вызванный повреждением крупных сосудов, в течение нескольких часов может привести к смерти от острой кровопотери, поэтому в большинстве случаев при большое Г. и при Г. с продолжающимся кровотечением показана экстренная торакотомия с ушиванием раны легкого или перевязкой сосуда.
В зависимости от показателей свертывающей и фибринолитической систем у больных с кровотечением в плевральную полость в ближайшем послеоперационном периоде после радикальных вмешательств на легких применяет ε-аминокапроновую к-ту, протаминсульфат, трасилол, фибриноген, введение одногруппной плазмы и других средств гемостаза под контролем величин концентрации фибриногена, времени свертываемости крови и показателей фибринолитической активности (В. Т. Плешаков, 1969). При неэффективности их показана реторакотомия для остановки кровотечения. Для возмещения кровопотери допустима реинфузия излившейся в плевральную полость крови, но только при травмах без значительного повреждения легочной ткани, когда нет признаков инфицирования крови, и не. позже 12 час, после травмы.
Прогноз и профилактика
Успешность лечения гемоторакса определяется характером травмы или заболевания, интенсивностью кровопотери и своевременностью хирургической помощи. Прогноз наиболее благоприятен при малом и среднем неинфицированном гемотораксе. Свернувшийся гемоторакс повышает вероятность развития эмпиемы плевры. Продолжающееся внутриплевральное кровотечение или одномоментная большая кровопотеря могут привести к гибели пациента.
Исходом гемоторакса может являться образование массивных плевральных сращений, ограничивающих подвижность купола диафрагмы. Поэтому в период реабилитации пациентам, перенесшим гемоторакс, рекомендуются занятия плаванием и дыхательной гимнастикой. Профилактика гемоторакса заключается в предупреждении травматизма, обязательной консультации пациентов с торакоабдоминальной травмой хирургом, контроле гемостаза при операциях на легких и средостении, осторожном выполнении инвазивных манипуляций.
Этиология и патогенез
Наиболее частой причиной Г. являются повреждения легких. По данным В. И. Колесова (1949), частота Г. в Великую Отечественную войну при проникающих ранениях груди варьировала в пределах 55—80%. В мирное время, по E. М. Вагнеру (1969), при закрытых травмах груди, сопровождающихся повреждением легких, Г. наблюдается у 25,9% больных; чаще он бывает (30,2%) при травмах с повреждением костей, чем без повреждений их (12,4%). После любой трансплевральной операций имеет место послеоперационный Г., что не является осложнением, но в некоторых случаях послеоперационный Г. может приобретать самостоятельное значение. В этих случаях речь идет или о внутриплевральном кровотечении или о свернувшейся Г. Крайне редко Г. может быть осложнением плевральных пункций. Помимо травмы, Г. может развиться как осложнение некоторых заболеваний (туберкулез легких, новообразования легких, плевры, средостения или грудной стенки, аневризмы крупных внутригрудных сосудов, геморрагический диатез и др.).
Г. образуется при нарушении целости или увеличений проницаемости сосудов легких, плевры или грудной стенки и средостения. При травмах чаще других повреждаются сосуды легких. Количество крови, изливающейся в плевральную полость; зависит от степени разрушения легкого и локализации ранения. Повреждения периферических отделов лёгкого обычно сопровождаются малым иди средним Г.; ранения в области корня Легкого с повреждением магистральных сосудов сопровождаются массивным и быстрым кровотечением (большой Г.) и почти всегда смертельны.
Уже в первые часы пребывания в плевральной полости кровь вызывает реакцию плевральных листков — асептическое воспаление плевры, так наз. гемоплеврит. Сначала состав излившейся в плевральную полость крови почти не отличается от периферической крови, но постепенно количество гемоглобина в ней снижается, эритроцитарно-лейкоцитарный индекс уменьшается. Обычно кровь в плевральной полости не свертывается, однако постепенно происходит выпадение отдельных компонентов тромбообразованию и наступает процесс фибринолиза. Кроме этого, в крови, истекающей из лёгкого, содержатся антикоагулирующие вещества, что также препятствует свертыванию крови. В тех случаях, когда кровотечение очень сильное, может наблюдаться свертывание крови (чем больше крови изливается в плевральную полость в единицу времени, тем больше образуется сгустков); способность свертываться кровь сохраняет лишь в течение 4—5 час, после прекращения кровотечения.
Патол, изменения плевры при Г. характеризуются отечностью и умеренной лейкоцитарной инфильтрацией, в основном соединительнотканных ее слоев; имеет место также набухание, дискомплексация и слущивание клеток мезотелия. В более поздние сроки (после третьих суток) появляются инфильтрация полибластами и пролиферация фибробластов.
Сдавление легкого, особенно выраженное при среднем и большом Г., а также при гемопневмотораксе, сопровождается уменьшением дыхательной поверхности легкого и усугубляет расстройства дыхания и кровообращения. Смещение средостения со сдавлением полых вен и легочных сосудов в свою очередь оказывает неблагоприятное влияние на гемодинамику. Особенно это выражено при открытом гемопневмотораксе, сопровождающемся флотацией средостения и плевро-пульмональным шоком.
Классификация
В соответствии с этиологией различают травматический, патологический и ятрогенный гемоторакс. С учетом величины внутриплеврального кровотечения гемоторакс может быть:
- малый - объем кровопотери до 500 мл, скопление крови в синусе;
- средний - объем до 1,5 л, уровень крови до нижнего края IV ребра;
- субтотальный - объем кровопотери до 2 л, уровень крови до нижнего края II ребра;
- тотальный - объем кровопотери свыше 2 л, рентгенологически характеризуется тотальным затемнением плевральной полости на стороне поражения.
Количество крови, излившейся в плевральную полость, зависит от локализации ранения и степени разрушения сосудов. Так, при повреждении периферических отделов легкого, в большинстве случаев возникает малый или средний гемоторакс; при ранениях корня легкого обычно повреждаются магистральные сосуды, что сопровождается массивным кровотечением и развитием субтотального и тотального гемоторакса.
Кроме этого, также выделяют ограниченный (обычно малый по объему) гемоторакс, при котором излившаяся кровь скапливается между плевральными спайками, на изолированном участке полости плевры. С учетом локализации ограниченный гемоторакс бывает верхушечным, междолевым, паракостальным, наддиафрагмальным, парамедиастинальным.
В случае продолжающегося внутриплеврального кровотечения говорят о нарастающем гемотораксе, в случае прекращения кровотечения - о ненарастающем (стабильном). К осложненным видам относят свернувшийся и инфицированный гемоторакс (пиогемоторакс). При одновременном попадании в полость плевры воздуха и крови, говорят о гемопневмотораксе.
Лечение гемоторакса
Пациенты с гемотораксом госпитализируются в специализированные хирургические отделения и находятся под наблюдением торакального хирурга. С лечебной целью для аспирации/эвакуации крови производится дренирование плевральной полости с введением в дренаж антибиотиков и антисептиков (для профилактики инфицирования и санации), протеолитических ферментов (для растворения сгустков). Консервативное лечение гемоторакса включает проведение гемостатической, дезагрегантной, симптоматической, иммунокорригирующей, гемотрансфузионной терапии, общей антибиотикотерапии, оксигенотерапии.
Малый гемоторакс в большинстве случаев может быть ликвидирован консервативным путем. Хирургическое лечение гемоторакса показано в случае продолжающегося внутриплеврального кровотечения; при свернувшемся гемотораксе, препятствующем расправлению легкого; повреждении жизненно важных органов.
В случае ранения крупных сосудов или органов грудной полости производится экстренная торакотомия, перевязка сосуда, ушивание раны легкого или перикарда, удаление излившейся в плевральную полость крови. Свернувшийся гемоторакс является показанием к плановому выполнению видеоторакоскопии или открытой торакотомии для удаления сгустков крови и санации плевральной полости. При нагноении гемоторакса лечение проводится по правилам ведения гнойного плеврита.
МКБ-10
J94.2 Гемоторакс
Содержание
Свернувшийся гемоторакс
Свертывание крови в плевральной полости (свернувшийся Г.) и образование нитей фибрина в плевральном экссудате (фибриноторакс) сопровождаются формированием многокамерной полости, что затрудняет ее опорожнение и способствует развитию эмпиемы плевры. При массивном свернувшемся Г. развивается компрессионный ателектаз легкого, что ведет к появлению дыхательных и гемодинамических расстройств.
Свернувшийся Г. отмечается при проникающих ранениях в 10—20% случаев в военное время, в 5—10% случаев — в мирное время; после плановых операций на легких и плевре — в 1,5 — 27,5% случаев (по данным разных авторов).
Кровь, излившаяся в плевральную полость после травм и оперативных вмешательств, может свернуться лишь в первые минуты после кровотечения. Если же кровь не свернулась в первые 5—15 мин., она оказывается дефибринированной и не свертывается даже после аспирации ее из полости. Основные условия формирования свернувшегося Г.: интенсивное кровотечение, при к-ром скорость поступления в полость крови превышает скорость процессов дефибринирования; наличие обширной раневой поверхности в полости, что способствует не только кровотечению из мелких сосудов, но и активно ускоряет свертывание изливающейся крови за счет выделения тромбопластина из поврежденных тканей; низкая фибринолитическая активность накапливающейся в полости крови; ограниченные движения диафрагмы, легкого и грудной стенки. Имеется прямо пропорциональная зависимость времени свертывания и массы образующихся сгустков от интенсивности кровотечения в полость и степени повреждения тканей грудной стенки легкого.
Кровяные сгустки, образующиеся в полости, могут самостоятельно разрушаться под влиянием фибринолитических компонентов излившейся крови, дыхательных движений и сердцебиения. Освобождающиеся при этом пучки фибрина оседают в нижних отделах полости плевры или прикрепляются к поврежденной поверхности грудной стенки и легкого. При массивном свернувшемся Г. часть сгустков постепенно уплотняется и прорастает фибробластами со стороны плевры. В результате ретракции и организации сгустков образуется множество мелких изолированных камер.
Значительная экссудация в плевральную полость неизбежна даже при асептическом течении Г., что приводит к развитию гемоплеврита. Определяющим условием разграничения плеврального экссудата фибринными пленками с образованием уровней жидкости является наличие в ней способного свертываться фибриногена (св. 10 мг%). Нередко фибриноторакс может быть следствием экссудативного плеврита и при неправильном лечении приводит к образованию плотных массивных сращений и к нарушению функции внешнего дыхания.
В первые дни клин, симптомы при свернувшемся Г. определяются величиной кровопотери (см.) (признаки острого внутреннего кровотечения), а также степенью сдавления легкого (см. Ателектаз) и органов средостения (притупление легочного звука, ослабленное дыхание, гемодинамические и дыхательные нарушения). В последующем повышается температура тела, усиливается недомогание и боли в груди, нарастает экссудация в плевральную полость, увеличивается число лейкоцитов в циркулирующей крови и в плевральном экссудате. По сводным данным отечественных и зарубежных авторов, у 36% больных со свернувшимся Г. развивается эмпиема плевры (см. Плеврит). Но при асептическом течении свернувшегося Г. и фибриноторакса возможны иные осложнения — значительные стойкие расстройства внешнего дыхания (вследствие развития соединительнотканного рубца — фиброторакса).
Объем и характер леч. мероприятий определяются общим состоянием больного, степенью повреждения легкого и грудной стенки, величиной кровопотери. С целью предупреждения эмпиемы плевры и развития массивных плевральных сращений должна проводиться санация плевральной полости. Однако пункции плевры при свернувшемся Г. и фибринотораксе малоэффективны, т. к. удается аспирировать лишь незначительное количество жидкости. Введением антибиотиков в плевральную полость часто не удается предупредить эмпиему, т. к. трудно определить, в какой из изолированных камер полости развивается инфекция. Калинер (М. М. Culiner) с соавт. (1959), В. И. Маслов (1976) и др. предлагают промывать плевральную полость антисептическими р-рами, чтобы «размыть» разграничивающие полость сгустки. По-видимому, это возможно лишь при разграничении полости тонкими пленками фибрина. При наличии в полости сгустков крови или большого количества фибрина удаление их промываниями и аспирацией невозможно. Поэтому большинство хирургов считает, что в таких случаях показана торакотомия (см.). Однако оперативное удаление сгустков может предотвратить развитие эмпиемы плевры лишь в том случае, если его выполняют в ближайшие дни после формирования свернувшегося Г. Если сгустки удалены на 2—3-й нед. после травмы, то почти у половины больных после торакотомии развивается эмпиема.
Из ферментных препаратов для лечения свернувшегося Г. и фибриноторакса наиболее эффективны стрептолиаза, террилитин, фибринолизин, химотрипсин, трипсин, химопсин и др. Свойство стрептокиназы проникать внутрь сгустка и активировать фибринолиз способствует более полному лизису сгустков.
Во многих случаях целесообразно применять активаторы фибринолиза в комбинации с фибринолитическими препаратами прямого действия (фибринолизин, химотрипсин и др.). Самостоятельное применение фибринолизина, а тем более химотрипсин при свернувшемся Г. менее эффективно. Эти препараты можно использовать для лизиса отдельных фибринных пленок при фибринотораксе, чтобы уменьшить количество изолированных камер в плевральной полости и создать более благоприятные условия для санации ее при угрозе развития эмпиемы.
Наиболее оптимальные сроки для проведения фибринолитической терапии — 4—10-й день после формирования свернувшегося Г. В первые дни после травмы применение ферментов нежелательно из-за опасности развития повторного кровотечения.
Противопоказания к внутриплевральному применению фибринолитических препаратов — продолжающееся кровотечение, значительная аллергизация организма и подозрение на наличие бронхиального свища. При неэффективности фибринолитической терапии свернувшегося Г. и фибриноторакса показано оперативное вмешательство.
Библиография: Вагнер Е. А. Хирургическое лечение проникающих ранений груди в мирное время, ДО., 1964, библиогр.; он же, Проникающие ранения груди, М., 1975; библиогр.; Неотложная хирургия, под ред. Н. И. Блинова и Б. М. Хромова, Д., 1970, библиогр.; Опыт советской медицины в Великой Отечественной войне 1941—1945 гг., т. 9—10, М., 1949—1950
Свернувшийся гемоторакс - Григорян А. В. и др. Бактериальные ферменты в лечении гнойной инфекции, Сов. мед., № 12, с. 39, 1967, библиогр.; Колесников И. С. Лечение раненных в грудь со свернувшимся гемотораксом, Вестн, хир., т. 75, № 2, с. 16, 1955; Костюченко А. Л. и Чепчерук Г. С. Превентивная санация плевральной полости после пневмонэктомии с использованием фибринолитических препаратов, Клин, хир., № 11, с. 23, 1975, библиогр.; Маслов В. И. Лечение эмпием плевры, Л., 1976, библиогр.; Beall А. С., Crawford H. W. а. De Bekey М. E. Considerations in the management of acute traumatic hemothorax, J. thorac. cardiovasc. Surg., v. 52, p. 351, 1966; Cosgriff S. W. Study of coagulation mechanism of pleural blood in hemopneumothorax, Amer. J. Med., v. 8, p. 57, 1950; Culiner М. М., R o e В. В. a. Grimes O. F. The early elective surgical approach to the treatment of traumatic hemothorax, J. thorac. cardiovasc. Surg., v. 38, p. 780, 1959.
В. М. Сергеев, Г. Б. Катковский; И. С. Колесников, М. И. Лыткин, Г. С. Чепчерук
Гемоторакс (Haemothorax) - скопление крови в плевральной полости.
У животных чаще встречается односторонний гемоторакс.
Этиология. К гемотораксу у животных могут привести проникающие ранения грудной стенки, разрыве межреберных артерий, внутренней грудной артерии, аорты и других кровеносных сосудов, ранения легких, переломы ребер и грудной кости и ряд заболеваний: туберкулез легких, новообразования, абсцесс, аневризма, диатез. У рогатого скота гемоторакс бывает при ранениях плевры и легких острыми инородными предметами со стороны преджелудков (травматический ретикулит).
Наиболее опасными для жизни животных являются ранения крупных сосудов корня легкого, аорты и сердца.
Патогенез. Скопление крови в плевральной полости сопровождается у животного реактивным воспалением плевры. В начале излившаяся кровь по своему составу ничем не отличается от периферической. Начиная с первых суток, к крови примешивается экссудат, снижается содержание гемоглобина и эритроцитов, увеличивается число лимфоцитов и моноцитов, иногда эозинофилов. Содержимое плевральной полости долго остается жидким, затем принимает серозно-геморрагический характер и постепенно начинает рассасываться. При попадание гноеродной микрофлоры содержимое принимает мутный оттенок с наличием сгустков крови и фибрина.
Клиническая картина. Животное возбуждено, проявляет беспокойство, мышечная дрожь, у него усиливается общая слабость, шаткая походка и угнетение. Болевые рефлексы понижены. Температура тела у такого животного нормальная или несколько понижена, наступает похолодание периферических частей тела, при развитии гемоплеврита температура тела может повышаться до субфебрильной (температура тела повышается до 1°С выше нормы) или фебрильной (температура тела повышается более 1°С). При неблагоприятном течении болезни у больного животного прогрессивно развивается дыхательная недостаточность, дыхание становится учащенным и напряженным, появляется бледность и цианоз видимых слизистых оболочек. Пульс учащенный, слабого наполнения, сердечный толчок усиливается, тоны сердца при аускультации усилены и глуховаты. Перкуссией грудной стенки отчетливо обнаруживают горизонтальную границу притупления в нижней части груди, как при экссудативном плеврите, небольшое смещение сердца, ниже границы притупления дыхательные шумы при аускультации легких не прослушиваются. При нарушении целостности кровеносных сосудов легких у больного животного регистрируют кровянисто - пенистое истечение из носовых отверстий, которое усиливается во время кашля. В том случае, когда гемоторакс у животного возникает на почве туберкулеза, абсцесса, новообразования, геморрагического диатеза, появляется кашель с примесью крови в мокроте. При лабораторном исследовании крови - резкое уменьшение количества эритроцитов и гемоглобина.
Прогноз. При малых кровотечениях в плевральную полость происходит их резорбция в течение 1,5 -3 недель. При больших кровоизлияниях рассасывание излившейся крови из плевральной полости происходит медленно, кровь может свернуться. При попадание в плевральную полость патогенной микрофлоры, заболевание может осложниться плевритом, пневмонией, гангреной легких, сепсисом. При повреждении крупных кровеносных сосудов у животного может наступить летальный исход от острой анемии.
Диагноз устанавливают на основании анамнеза, клинических признаков и диагностической пункции плевральной полости. Рентгенологическим исследованием устанавливают затенение нижних отделов легочного поля с колеблющейся верхней горизонтальной границей.
Дифференциальный диагноз. Исключаем плеврит, гидроторакс и пневмоторокс.
Лечение. В острых случаях заболевания для уменьшения кровотечения внутривенно вводят 10% раствор хлористого кальция или хлорида натрия, подкожно в нескольких местах вводят лошадиную сыворотку, делают переливание совместимой крови. В экстренных случаях больному животному переливают кровь без определения ее совместимости, предварительно стабилизировав ее салицилатом натрия (для лошадей 10% раствор- 2:10, рогатого скота - 3:10). Для остановки кровотечения ветеринарные специалисты применяют викасол - крупным животным по 0,1 -0,3г 2-3 раза в день, собакам доза викасала составляет - 0,01- 0,03г.
Дополнительно больным животным применяют кровезаменители (полиглюкин, гемодес), подкожно вводят аминокислоты.
После остановки кровотечения из плевральной полости часть скопившейся крови или экссудата удаляют пункцией. В случае нарастающего гемоплеврита пункцию плевры повторяют через 1-2 дня. При гнойном плеврите назначают подтитрованные в ветеринарной лаборатории антибиотики. С целью профилактики пневмонии больному животному некоторые ветеринарные специалисты делают шейную ваго - симпатичную блокаду раствором новокаина.
Профилактика. Профилактика гемоторакса у животных строится на устранение причин, которые приводят к гемотораксу. В местах нахождения животных убирают все острые и посторонние предметы, которые способны травмировать грудную клетку. Владельцы животных и обслуживающий персонал должны более тщательно контролировать погрузку и транспортировку животных.
Гидрото́ракс (гемоторакс)— скопление жидкости невоспалительного происхождения (транссудата) в плевральной полости.
Классификация: Малый гемоторакс - кровь в пределах реберно-диафргмальнго синуса, средний - скопление крови от угла до уровня средины лопатки, большой - уровень крови выше середины лопатки.
Клиника: Одышка. Цианоз. Отставание больной половины грудной клетки при дыхании. Увеличение в объеме одной половины грудной клетки. Вынужденное положение пациента на больном боку.
Наряду с пневмотораксом, гидроторакс может стать причиной компрессионного ателектаза - сжатия легкого с потерей им воздушности и способности к осуществлению дыхательных движений, что проявляется одышкой и сухим кашлем, т.е. развивается острая недостаточность дыхательной функции;
Диагностика. Ведущими методами исследования, помимо специфических объективных данных, являются рентгенография грудной клетки в различных проекциях, пункция плевральной полости и торакоскопия. Рентгенологическими симптомами повреждения легкого являются признаки подкожной и межмышечной эмфиземы (светлые полоски газа в мягких тканях грудной клетки), пневмо- или гидроторакс, различные изменения бронхо-легочной структуры. Показанием к пункции плевральной полости является предполагаемое наличие в ней воздуха или жидкости (кровь, эксудат). При наличии воздуха в плевральной полости место пункции зависит от общего состояния больного. Если больной может сидеть, пункцию проводят во втором межреберье по среднеключичной линии. Если больной сидеть не может, а лежит — то в пятом-шестом межреберье, по среднеподмышечной линии. Для удаления жидкости или крови пункцию производят в шестом-седьмом межреберье между задней и средней подмышечной линиями (в положении сидя) или ближе к задней подмышечной линии (в положении лежа). Пункцию производят по верхнему краю ребра во избежание повреждения межреберных сосудов. Торакоскопия используется при закрытых повреждениях, осложненных травматическим пневмотораксом, для уточнения характера повреждения и выбора рациональной лечебной тактики.
Лечение гидроторакса
При гидротораксе, обусловленном наличием у больного сердечной недостаточности, рекомендуют больному оптимизацию режима труда и отдыха. Медикаментозное лечение может быть направлено на усиление сниженной сократительной способности миокарда (назначают сердечные гликозиды, стимуляторы β-адренорецепторов, ингибиторы фофодиэстеразы), выведение излишнего количества жидкости из организма назначением мочегонных препаратов (ингибиторы карбоангидразы, «петлевые», тиазидовые и тиазидоподобные, калийсберегающие диуретики), уменьшение нагрузки на левый желудочек сердца (периферические венозные, артериальные и смешанные сосудорасширяющие средства, ингибиторы АПФ).
При развитии гидроторакса, который обусловлен заболеваниями почек, сопровождающимися развитием нефротического синдрома (гломерулнефрит, амилоидоз почек), рекомендуют постельный режим, соблюдение которого способствует увеличению выработки мочи. Проводят коррекцию нарушений белкового обмена, для чего обеспечивают оптимальное содержание белка в пище, назначают средства, способствующие уменьшению потерь белка с мочой (ингибиторы АПФ), при необходимость переливают 20% раствор альбумина (по 100-150 мл 1 раз в 2-3 дня курсом до 5-6 вливаний); назначают мочегонные средства (тиазидовые, «петлевые», калийсберегающие диуретики).
При значительном скоплении жидкости в плевральной полости, приводящем к сдавлению лёгких и развитию дыхательной недостаточности, прибегают к плевральной пункции с медленным удалением транссудата из плевральной полости. Эта лечебная манипуляция является одновременно и диагностической, так как характер полученной жидкости и результаты её лабораторного исследования позволяют отличить гидроторакс от экссудативного плеврита, гемоторакса, эмпиемы плевры.
Плевральную пункцию производят в положении больного сидя с опорой на руки перед собой под местной анестезией, как правило, в наиболее низкой точке плевральной полости. Используется специальная длинная и толстая пункционная игла. Типичным местом для пункции является восьмое межреберье по задней поверхности грудной клетки. В области прокола тонкой иглой послойно вводят в мягкие ткани 0,5 раствор новокаина, объёмом 10-15 мл, после чего врач вводит в плевральную полость пункционную иглу, через которую медленно отсасывает жидкость. Рекомендуется одновременно удалять не более 1,5 литров жидкости, так как эвакуация большего количества может вызвать быстрое смещение органов средостения и падение артериального давления. После удаления иглы место прокола заклеивается стерильной повязкой.
Освобождение плевральной полости от транссудата приводит к облегчению дыхания и способствует нормализации кровообращения. Плевральная пункция считается относительно несложной манипуляцией, не требующей от пациента никакой предварительной подготовки и не накладывающей каких-либо существенных ограничений на него после её проведения. На следующий день после пункции обязательно выполнение контрольной рентгенографии лёгких для исключения возможных осложнений плевральной пункции (пневмоторакс вследствие прокола лёгкого). При рецидивирующем характере гидроторакса по показаниям прибегают к повторным пункциям плевральной полости, иногда неоднократным.
(ДВС-синдром)-нарушение гемостаза, в основе которого лежит распространенное свертывание крови с образованием большого количества микросгустков и агрегатов клеток крови, что приводит к нарушению микроциркуляции в органах и тканях, развитию выраженных дистрофических изменений.
Этиология. ДВС-синдром развивается при различных ситуациях — хирургических вмешательствах, акушерской патологии, сепсисе, злокачественных опухолях, а также при некоторых терапевтических заболеваниях и состояниях — гемобластозах, острой и хронической почечной недостаточности, системных васкулитах, остром гемолизе.Патогенез. Изменение состояния свертывающей и противосвертывающей систем при развитии ДВС-синдрома проходит несколько стадий.В начальной стадии (стадия гиперкоагуляции) под влиянием различных экзогенных (продукты жизнедеятельности бактерий, змеиные яды, трансфузионные средства и пр.) и эндогенных (продукты протеолиза и цитолиза, тканевый тромбопластин и др.) факторов активируются процессы свертывания крови и агрегации тромбоцитов.Затем происходит выпадение тромбов, чему способствует также попадание в кровоток большого количества продуктов белкового распада под влиянием одновременной активации других систем — фибринолитической, калликреин-кининовой. Множественное тромбообразование приводит к нарушению микроциркуляции и изменениям функций различных органов и систем.
Активация свертывания крови вызывает истощение противосвертывающих механизмов-
физиологических антикоагулянтов (системы «гепарин — антитромбин III») и фибринолитической системы «плазминоген-плазмин». Множественное тромбообразование влечет за собой так назы-ваемую коагулопатию потребления (снижение содержания плазменных факторов свертывания) и тромбоцитопению, что обусловливает развитие геморрагического синдрома.
Принято различать острый ДВС-синдром (развитие идет в пределах су¬ток), подострый (развивается в течение нескольких суток — недели), хро¬нический (протекает многие недели и месяцы). В течении ДВС-синдрома условно выделяют четыре стадии: 1) гиперкоагуляция и агрегация; 2) переходная с нарастающей коагуляцией, тромбоцитопенией и разнонаправленными сдвигами в различных коагуляционных тестах; 3) гипокоагуляция; 4) восстановительная.
Лечение. Лечение ДВС-синдрома должно включать мероприятия, направленные на устранение причины его развития (лечение инфекционных процессов, основного заболевания), борьбу с шоком, коррекцию гемостаза.•Трансфузии свежезамороженной плазмы — один из основных мето¬дов лечения острого ДВС-синдрома (гепарин добавляют для того, чтобы плазма не свернулась). Свежезамороженная плазма содержит антитромбин III, плазминоген, факторы свертывания и естественные антиагреганты. •Массивные трансфузии свежезамороженной плазмы осуществляют под прикрытием профилактических доз гепарина по 2500—5000 ЕД 2 раза в сутки подкожно. В настоящее время используют также низкомолекулярный гепарин — фраксипарин по 0,3—0,5 мл подкожно или клексан по 40 мг/сут подкожно. При резкой активации фибринолиза необходимо введение 100 000 ЕД/сут контрикала или других антипротеаз в максимальных Дозах. При профузных маточных, носовых, желудочно-кишечных, легоч¬ных кровотечениях внутривенно вводят тромбоконцентраты. Локальная остановка кровотечений — тампонады, перекись водорода, ПАМБА, ами-нокапроновая кислота, дицинон (этамзилат) в виде аппликаций, турунд, смоченных раствором дицинона (в нос), внутрь и парентерально.В настоящее время используют супернатантную плазму, имеющую меньшую тенденцию к свертыванию, чем свежезамороженная плазма, в ней содержится меньше фибриногена, фактора VIII, фибронектина и фак¬тора Виллебранда. Таким образом, появилась возможность замещения ес¬тественных физиологических антикоагулянтов при массивных тромбозах.
• Плазмаферез и плазмозамену, позволяющие удалять активность свертывания и продукты паракоагуляции, широко используют при иммунокомплексном синдроме, тканевом распаде, некрозе, выраженном геморрагиче¬ском синдроме, септическом шоке, ожогах, при синдроме раздавливания тканей, улучшают гемодинамику, предупреждают развитие острой почеч¬ной недостаточности.
• При выявлении бактериемии (в большинстве случаев острого ДВС-синдрома) необходимо назначать антибиотики (не очень токсичные) для стерилизации кишечника.
• Трансфузии эритроцитной массы осуществляют в редких случаях — лишь при острой кровопотере (более 1 л крови), так как в крови донора содержится много активаторов свертывания крови.
• Для защиты эндотелия от бактериальных эндотоксинов используют эндотелиопротекторы (интерлейкины, цитокины, факторы некроза опухо¬лей, медиаторы воспаления).
Гемоторакс - это кровотечение в полость плевры, скопление крови между ее листками, приводящее к сдавлению легкого и смещению органов средостения в противоположную сторону. При гемотораксе отмечается боль в грудной клетке, затруднение дыхания, развиваются признаки острой кровопотери (головокружение, бледность кожных покровов, тахикардия, гипотония, холодный липкий пот, обмороки). Диагностика гемоторакса основана на физикальных данных, результатах рентгеноскопии и рентгенографии грудной клетки, КТ, диагностической плевральной пункции. Лечение гемотракса включает гемостатическую, антибактериальную, симптоматическую терапию; аспирацию скопившейся крови (пункции, дренирование плевральной полости), при необходимости - открытое или видеоторакоскопическое удаление свернувшегося гемоторакса, остановку продолжающегося кровотечения.
Читайте также:
- Ротвейлер: отзывы владельцев, описание породы, особенности содержания, плюсы и минусы, отношение к детям и домашним животным
- О продолжительности жизни русских спаниелей дома: влияющие факторы
- Далматинец - звездный пес, прирожденный артист и любимец детей
- Кандидоз у кур, бройлеров и цыплят: симптомы, лечение, препараты, меры профилактики
- Отравление у лошади: признаки, первая помощь, лечение

